
Granuloma de Majocchi – reporte de caso.
Majocchi´s granuloma – case report.
Hari Teresa Martínez Rivas1, Samaria Sirias2
1 Patóloga. Hospital Salud Integral, Managua.
harimartnezrvas@gmail.com https://orcid.org/0000-0002-5815-0939
2Dermatóloga. Centro Médico Quirúrgico Santa Gema, Masaya.
samaria_011683@hotmail.com, https://orcid.org/0000-0002-0904-6035
RESUMEN
El granuloma dermatofítico, conocido también como Granuloma de Majocchi (GM) se caracteriza por inflamación granulomatosa, perifolicular. Fue descrita por Domenico Majocchi (1883). El GM es una entidad rara producida por dermatofitos que provoca una infección profunda de la dermis y tejido celular subcutáneo, aunque en la descripción inicial fue relacionada con Trichophyton tonsurans, se reportaron posteriormente otros agentes etiológicos no-dermatofitos (Phoma, Aspergillus, Malbranchea). Aparece tanto en individuos sanos como inmunocomprometidos y se caracteriza por nódulos, placas y pápulas que afectan áreas expuestas a trauma. Generalmente, afecta extremidades superiores e inferiores (antebrazos, manos, piernas y rodillas o tobillos), y ocasionalmente, aparece en piel cabelluda y cara. El diagnóstico clínico debe complementarse con estudios micológicos y citológicos y confirmados histológicamente con la presencia de inflamación granulomatosa perifolicular. No hay respuesta a la terapia tópica antifúngica y, por lo tanto, requiere terapia sistémica. A continuación, se describe caso clínico en un niño de 6 años de edad con afectación facial, que se presentó con una lesión tipo placa que afectó nariz, con un mes de evolución. Se realizó biopsia diagnóstica que detectó la infección profunda por hongos; siendo tratado con terbinafina con respuesta completa.
Palabras claves: Granuloma de Majocchi; tiña; terbinafina.
ABSTRACT
Dermatophytic granuloma, also known as Majocchi's Granuloma (GM) is characterized by granulomatous, peripollicular inflammation. It was described by Domenico Majocchi (1883). GM is a rare entity produced by dermatophytes that causes a deep infection of the dermis and subcutaneous cellular tissue, although in the initial description was related to dermatophyte Trichophyton tonsurans, other non-dermatophyte etiological agents (Phoma, Aspergillus, Malbranchea) were subsequently reported. GM appears in both healthy and immunocompromised individuals and is characterized by nodules, plaques, and papules that affect areas exposed to trauma. Generally, it affects upper and lower extremities (forearms, hands, legs, and knees or ankles), and occasionally, it appears on the scalp and face. The clinical, mycologic, and/or cytologic diagnosis should be confirmed by the demonstration of perifollicular granulomatous inflammation by histologic examination. There is no response to topical antifungal therapy and therefore requires systemic therapy. The following describes a clinical case in a 6-year-old boy with facial involvement, who presented a plaque-like lesion that affected the nose, with a month of evolution. A diagnostic biopsy was performed that detected deep fungal infection; being treated with terbinafine with complete response.
Key words: Majocchi's granuloma; tinea; terbinafine
INTRODUCCIÓN
El Granuloma de Majocchi (GM) fue descrito por primera vez por el dermatólogo italiano Domenico Majocchi en 18831,2. El GM es una infección micótica rara que se caracteriza por lesiones tipo nódulos o placas a nivel de miembros inferiores, a menudo en mujeres que se afeitan, aunque también puede aparecer en niños3. Otras regiones afectadas incluyen cara, ingle, escroto y vulva4. Se ha visto asociado a Trichophyton rubrum, Microsporum canis, Trichophyton violaceum, Trichophyton tonsurans, Trichophyton mentagrophytes y Aspergillus fumigatus4. Usualmente aparece en individuos inmunocompetentes. Como consecuencia de lesiones al folículo piloso, los hongos (usualmente con detritos de queratina) son liberados hacia el tejido circundante, donde producen una respuesta inflamatoria intensa. En algunos casos, los pacientes pueden tener un estado de inmunocompromiso asociado al uso de corticoterapia, que afecta las reacciones de hipersensibilidad retardada. En este tipo de pacientes inmunodeprimidos se ha descrito, muy raras veces, una forma diseminada, denominada Enfermedad de Majocchi.4
REPORTE DEL CASO
Paciente masculino, de 6 años de edad, blanco, procedente de Masaya, que al examen físico presentaba una dermatosis localizada en cabeza, afectando cara en dorso de nariz; constituida por una placa eritematosa con bordes infiltrativos, con escama adherida en el centro, de aproximadamente 1cm de diámetro mayor, que asienta sobre piel aparentemente sana. Contaba con un mes de evolución; sin síntoma del estado general y se asoció a ligero prurito (Figura 1).
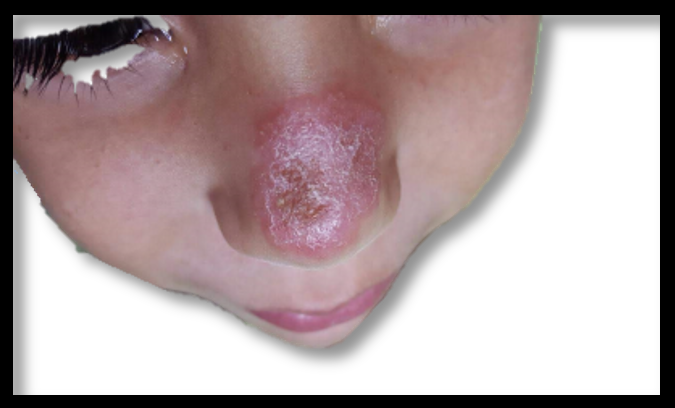
Fuente: Archivo de las autoras
El paciente recibió tratamiento antibiótico sin mejoría. Por lo cual, se decidió tomar biopsia de la lesión para descartar sarcoidosis. Los hallazgos morfológicos mostraron un patrón nodular granulomatoso y supurativo, que rodeaba e infiltraba los folículos pilosos y, en uno de ellos a nivel del tallo piloso, se identificaron esporas (Figura 2).
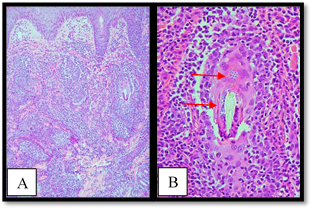
Fuente: Archivo de las autoras B-50-17.
De acuerdo a la histopatología fue compatible con perifoliculitis granulomatosa nodular por hongos (Granuloma de Majocchi). El tratamiento que se instauró de acuerdo al diagnóstico histológico fue terbinafina 250mg/día por 8 semanas con el cual hubo remisión completa de la enfermedad (Figura 3).
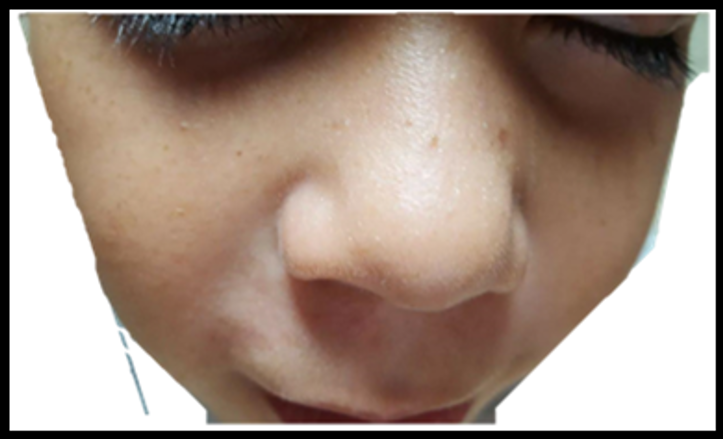
Fuente: Archivo de las autoras
Comentarios adicionales
En edades pediátricas la localización más frecuente es cabeza causado por el uso de corticoides tópicos; mientras que, en adultos, se presenta en miembros inferiores debido a traumas por afeitado3.
Consideraciones éticas
Por medio de la firma de consentimiento informado por parte del tutor del paciente, se recibió autorización para toma de fotografías como parte de archivo clínico, durante la consulta. Así como para la toma de biopsia cutánea para diagnóstico anatomopatológico, y del uso de fotografías microscópicas del tejido procesado en parafina.
DISCUSIÓN
Los dermatofitos son hongos altamente especializados, queratinofílicos y queratinolíticos, que consisten en siete géneros, que incluyen Trichophyton, Microsporum, Epidermophyton y recientemente agregados Arthroderma, Paraphyton, Nannizzia y Lophophyton.5
De acuerdo a los datos de la OMS, uno de cada cinco personas en la faz de la tierra padece esta patología6. La incidencia de la dermatofitosis, su distribución y agente etiológico, dependen del área geográfica, tiempo de estudio, estatus social y económico de la población, zona climática, edad y presencia de mascotas.
En Nicaragua, el Ministerio de salud reportó en el 2019 que el 1.4% de las causas de egresos hospitalarios corresponden a infecciones de piel y tejido celular subcutáneo.7 No obstante, no se encontraron estudios o registros con valor estadístico en cuanto a micología y epidemiología que reporten casos de dermatofitosis.
A pesar que los dermatofitos son los hongos patógenos más comunes en todo el mundo, pasan inadvertidos, puesto que es muy raro observar presentación clínica de diseminación sistémica que ponga en peligro la vida del paciente. La resistencia farmacológica in vitro se ha observado en limitados casos y la mayoría de los fármacos antifúngicos efectivos están disponibles en la mayoría de los países.8
Los tipos de lesiones más comunes en pacientes con GM son los nódulos (63,5%), seguido de placas (43,5%), pápulas (24,3%), úlceras (3,5%), abscesos (2,6%).9 Aproximadamente, un tercio (29,6%) de los pacientes presentaron pústulas en estas lesiones. Se ha observado que el número de casos reportados se ha incrementado en los últimos seis años y en especial la afectación facial.8
El GM se ha clasificado en dos formas, dependiendo del estado del individuo afectado y de las características clínicas1-6,8,9. La primera forma se observa principalmente en individuos sanos (62,6%)9 y clínicamente se observa una pápula perifolicular, inducida por un trauma penetrante que afecta las extremidades inferiores. La segunda forma es la granulomatosa, relacionada a inmunosupresión (37,4%)9, que se caracteriza por una dermatosis nodular, que aparece en extremidades superiores.
Entre los agentes etiológicos descritos, el más frecuente es Trichophyton rubrum, seguido de Trichophyton violaceum, Trichophyton mentagrohytes, Microsporum audounii, Microsporum gyseum, Microsporum canis y Epidermophyton floccosum1-6,8-9. Sin embargo, muchos tipos de hongos se han reportado como agentes etiológicos, tales como T. interdigitale, Microsporum canis, Nannizzia gypsea, Epidermophyton floccosum y entre los agentes no-dermatofitos se reportó al Aspergillus spp10, Phoma11 y Malbranchea spp.8
En todos los casos se considera el trauma como antecedente que desencadena la dermatosis3-6,8-11 y además de tomar en cuenta el rasurado de piernas o áreas púbicas y el contacto sexual, se debe investigar la ocupación.8,9 Se han reportado pacientes con contacto animal, sugiriendo la exposición a los animales como un factor predisponente. También, se conoce que los pacientes con dermatofitosis preexistente, tienen mayor riesgo de desarrollar GM, como fuente primaria de origen.8
Aunque los mecanismos de patogénesis del GM no están bien definidos, existen algunas hipótesis, y están relacionadas con muchos factores asociados al huésped y al microorganismo.8
El primer y más importante factor del huésped es la barrera cutánea.12 Los traumas físicos de la piel, como el rasurado, rascado y la inmunosupresión permiten la invasión por hongos. Una vez dentro de la dermis, el hongo origina una respuesta inflamatoria de la cual se invisibilizan mediante las proteínas asociadas al dominio LysM, que encierra literalmente los fragmentos de quitina de la pared de los hongos, la señal indicadora de que el intruso está ingresando.13,14 Además el hongo tiene muchas enzimas como lipasas, esterasas y colágenas. También, se conoce que se excreta una gran cantidad de sulfito que degrada los componentes de la piel.15,16
La inhibición de la respuesta inmunológica celular e inflamatoria, es un elemento importante en la progresión de la enfermedad. Se ha observado que los dermatofitos pueden causar infecciones profundas e invasivas en condiciones de inmunosupresión; diseminada, congénita y adquirida. Las dermatofitosis se han visto asociadas a linfopenia, disminución del complemento C3 y C4 e hipogammaglobulinemia. También se ha reportado en pacientes con deficiencia de caspasa, autosómica-recesiva.17,18,19
El huésped tiene muchos mecanismos para controlar la infección, tales como las peptidasas antimicrobianas (catelicidinas, defensinas), que atacan al hongo y promueven la epidermopoyesis. Además, están las células NK, neutrófilos y macrófagos, que responden ante los dermatofitos. Por lo tanto, la terapia inmunosupresora disminuye la inmunidad celular y el rango de ingestión-destrucción de las esporas.8
El uso indiscriminado de esteroides tópicos y la consiguiente disminución de la defensa local, pueden favorecer la infección por hongos, y desencadenar el Granuloma de Majocchi.8 Los esteroides afectan las funciones de los macrófagos y neutrófilos y reducen la respuesta inmune mediada por Th1. Así como otras condiciones de inmunosupresión como la quimioterapia y terapia antineoplásica (inhibidores de factor de necrosis tumoral alfa, adalimumab, inhibidores BARF)20,21; transplantes de órganos y alotransplante de tejido facial.8
Los pacientes con VIH presentan con mayor frecuencia infecciones por dermatofitos, aunque no existe un consenso en cuanto al recuento de linfocitos y las dermatofitosis cutáneas.22,23
El diagnóstico se realiza mediante el examen micológico directo, cultivo e histopatología.1-6,8-11 El examen de KOH es, por sí mismo, insuficiente para distinguir dermatofitosis superficiales y profundas. Las tinciones especiales (PAS y Grocott) en el estudio microscópico son muy importantes; puesto que, la hematoxilina/eosina de rutina es limitada en aquellos casos con un número pequeño de elementos fúngicos.24,25,26 La tinción de PAS es de más fácil realización y tiene mayor sensibilidad y valor predictivo negativo. En pacientes inmucomprometidos, es posible que se requiera técnicas de base molecular, para identificar los hongos. Se ha usado la secuencia de ITS (internal transcribed spacer).5,24,27,28 Sin embargo, el cultivo es el único que permite tanto la detección como el reconocimiento de la especie eventualmente.
El diagnóstico histológico se realiza con la detección de los dermatofitos tanto en capas superficiales como en dermis, acompañado de inflamación granulomatosa perifolicular de tipo cuerpo extraño.1-6,8-14 Si no se encuentra evidencia de infección del folículo piloso, no puede diferenciarse el GM de otras infecciones invasivas por dermatofitos.9
En el caso que se presenta, la detección del hongo fue posible por técnica de rutina, aunque se realizaron tinciones de histoquímica no fue posible visualizarlo y es posible que se deba a la poca cantidad de elementos y los cortes al micrótomo del tejido que se realizaron para las tinciones especiales.
El diagnóstico diferencial del GM incluye aquellas enfermedades de curso crónico que se caracterizan por pápulas y nódulos eritematosos.8 Debido a la presentación clínica de dolor, se perciben como síntoma de infección bacteriana, y esta confusión conlleva al tratamiento antibiótico. Otras infecciones crónicas pueden ser consideradas tales como por micobacterias, toxoplasmosis diseminada, leishmaniasis cutánea.11 Cuando la lesión afecta la cara, puede imitar rosácea granulomatosa y granuloma facial. Otras patologías que se presentan como nódulos dolorosos incluyen eritema nodoso, tromboflebitis, eritema indurada de Bazin. En pacientes inmunosuprimidos, es importante hacer diagnóstico diferencial con enfermedades tumorales tales como Sarcoma de Kaposi29 y linfomas.
El tratamiento incluye fármacos antifúngicos tópicos y sistémicos. En general, la terbinafina (250mg/día) es el antifúngico sistémico de preferencia (40,8%).8,9 Otros antifúngicos usados son el itraconazol (100-200 mg/día) (36,8%),8,21,30 griseofulvina (250-500mg/día) (11,8%),31,32 ketoconazol (8,6%), voriconazol (1%),11 y posaconazol (1%).33 Cuando el agente causal no puede ser aislado, la terbinafina debería ser el primer fármaco de elección, puesto que los casos que son resistentes al itraconazol o la griseofulvina mostraron respuesta a la terbinafina.9 Los antifúngicos deben continuarses hasta que las lesiones estén completamente sanadas. Dependiendo de la severidad del cuadro clínico, la duración de la terapia varía de 1 a 6 meses.11,34 Las reacciones adversas que se han presentado por el uso de los antifúngicos señalados, son la pigmentación, cicatriz atrófica y alopecia.8
CONCLUSIONES
El Granuloma de Majocchi (GM) es una infección micótica rara que en la mayoría de casos está relacionado con trauma físico local de la piel, seguido de la disrupción de los folículos pilosos. También se puede originar de una infección previa por dermatofitos, exposición a animales o humanos infectados, o condiciones inmunosupresoras locales o sistémicas. Puede aparecer en individuos inmunocompetentes e inmunosuprimidos. El diagnóstico de infección por hongos, debe sospecharse ante la presencia de lesiones refractarias al tratamiento con terapia antibiótica adecuada. El tratamiento incluye antifúngicos locales y sistémicos a dosis y duración apropiadas.
RECOMENDACIONES
Para realizar el diagnóstico histológico se recomienda complementar con tinciones especiales como PAS y Grocott. De igual manera, puede utilizarse el examen micológico directo. Ambas técnicas auxiliares son de bajo costo y fácil realización. En pacientes inmunosuprimidos, pueden ser cruciales los métodos moleculares.
REFERENCIAS BIBLIOGRÁFICAS
- Majocchi D. Sopra una nuova tricofizia (granuloma tri-cofitico), Studi clinici e micologici. Bull R Acad MedRoma. 1883; 9:220–3.
- Coelho WS, Diniz LM, Sousa Filho JB, Castro CM. Case for diagnosis. Granuloma trichophyticum (Majocchi`s granuloma). An Bras Dermatol. 2009;84: 85-6.
- Weedon, D., Strutton, G., Rubin, A. I., & Weedon, D. Weedon's skin pathology. 5th ed. Edinburgh: Churchill Livingstone/Elsevier. 2021.
- Calonje, E. McKee's pathology of the skin: With clinical correlations. 5th ed. Elsevier. 2019.
- de Hoog, G. S., Dukik, K., Monod, M., Packeu, A., Stubbe, D., Hendrickx, M., Kupsch, C., Stielow, J. B., Freeke, J., Göker, M., Rezaei-Matehkolaei, A., Mirhendi, H., & Gräser, Y. (2017). Toward a Novel Multilocus Phylogenetic Taxonomy for the Dermatophytes. Mycopathologia, 182(1-2), 5–31. https://doi.org/10.1007/s11046-016-0073-9
- Nussipov Y, Markabayeva A, Gianfaldoni S, et al. Clinical and Epidemiological Features of Dermatophyte Infections in Almaty, Kazakhstan. Open Access Maced J Med Sci. 2017;5(4):409–413. Published 2017 Jun 19. doi:10.3889/oamjms.2017.124.
- Mapasalud.minsa.gob.ni [internet]. Nicaragua: Ministerio de salud; c2017 [consultado 2020 Sep 03]. Disponible en: http://mapasalud.minsa.gob.ni/mapa-de-padecimientos-de-salud-de-nicaragua.
- Boral H, Durdu M, Ilkit M. Majocchi's granuloma: current perspectives. Infect Drug Resist. 2018; 11:751–60.
- Durdu, M., Kandemir, H., Ilkit, M. et al. Changing Concepts and Current Definition of Majocchi's Granuloma. Mycopathologia 185, 187–192 (2020).
- Saadat P, Kappel S, Young S, Abrishami M, Vadmal MS. Aspergillus fumigatus Majocchi's granuloma in a patient with acquired immunode-ficiency syndrome. Clin Exp Dermatol. 2008;33(4):450–453.
- Ilkit M, Durdu M, Karakas ̧ M. Majocchi's granuloma: asymptom complex caused by fungal pathogens. Med Mycol.2012;50(5):449–57.
- Lee WJ, Kim JY, Song CH, et al. Disruption of barrier function in dermatophytosis and pityriasis versicolor. J Dermatol. 2011;38(11): 1049–1053.
- Sánchez-Vallet A, Saleem-Batcha R, Kombrink A, et al. Fungal effector Ecp6 outcompetes host immune receptor for chitin binding through intrachain LysM dimerization. Elife. 2013
- Martinez DA, Oliver BG, Gräser Y, et al. Comparative genome analysis of Trichophyton rubrum and related dermatophytes reveals candidate genes involved in infection. mBio 2012;3(5): e00259–12.
- Monod M. Secreted proteases from dermatophytes. Mycopathologia.2008;166(5–6):285–294.
- Zaugg C, Monod M, Weber J, et al. Gene expression profiling in the human pathogenic dermatophyte Trichophyton rubrum during growth on proteins. Eukaryot Cell. 2009;8(2):241–250
- Abdel-Rahman SM. Genetic predictors of susceptibility to dermato-phytoses. Mycopathologia. 2017;182(1–2):67–76.
- Alves de Medeiros AK, Lodewick E, Bogaert DJ, et al. Chronic and invasive fungal infections in a family with CARD9 deficiency. J Clin Immunol. 2016;36(3):204–209.
- Lanternier, F., Pathan, S., Vincent, Q. B., Liu, L., Cypowyj, S., Prando, C., et al. (2013). Deep dermatophytosis and inherited CARD9 deficiency. The New England journal of medicine, 369(18), 1704–1714. https://doi.org/10.1056/NEJMoa1208487
- Chou WY, Hsu CJ. A case report of Majocchi's granuloma associated with combined therapy of topical steroids and adalimumab. Medicine. 2016;95(2): e2245
- Anforth R, Carlos G, Eiris N, Clements A, Fernandez-Peñas P. Tinea hidden by a vemurafenib-induced phototoxic reaction in a patient with metastatic melanoma taking dexamethasone. Med J Aust. 2015; 203(1):41–42.
- Johnson RA. Dermatophyte infections in human immune deficiency virus (HIV) disease. J Am Acad Dermatol. 2000;43(Suppl 5):S135–142. Johnson RA. Dermatophyte infections in human immune deficiency virus (HIV) disease. J Am Acad Dermatol. 2000; 43(Suppl 5):S135–142.
- Rodwell GE, Bayles CL, Towersey L, Aly R. The prevalence of derma-tophyte infection in patients infected with human immunodeficiency virus. Int J Dermatol. 2008;47(4):339–343
- Su H, Li L, Cheng B, et al. Trichophyton rubrum infection characterized by Majocchi's granuloma and deeper dermatophytosis: case report and review of published literature. Mycopathologia. 2017;182(5–6):549–554.
- Reza Kermanshahi T, Rhatigan R. Comparison between PAS and GMS stains for the diagnosis of onychomycosis. J Cutan Pathol. 2010;37(10):1041–1044.
- Shiogama K, Kitazawa K, Mizutani Y, Onouchi T, Inada KI, Tsutsumi Y. New Grocott stain without using chromic acid. Acta Histochem Cytochem. 2015;48(1):9–14.
- Mirhendi H, Makimura K, de Hoog GS, et al. Translation elongation factor 1-α gene as a potential taxonomic and identification marker in dermatophytes. Med Mycol. 2015;53(3):215–224.
- Rezaei-Matehkolaei A, Mirhendi H, Makimura K, et al. Nucleotide sequence analysis of beta tubulin gene in a wide range of dermatophytes. Med Mycol. 2014;52(7):674–688
- Kim JE, Won CH, Chang S, Lee MW, Choi JH, Moon KC. Majocchi's granuloma mimicking Kaposi sarcoma in a heart transplant patient. J Dermatol. 2011;38(9):927–929
- Li FQ, Lv S, Xia JX. Majocchi's granuloma after topical corticosteroids therapy. Case Rep Dermatol Med. 2014;2014:507176.
- Kanaan IC, Santos TB, Kac BK, Souza AM, Cerqueira AM. Majocchi's granuloma – case report. An Bras Dermatol. 2015;90(2):251–253.
- Kranseler J, Gupta D. Erythematous annular plaques on a 9-year-old's arms and chest. Clin Pediatr. 2018;57(4):488–490.
- Jachiet, M., Lanternier, F., Rybojad, M., Bagot, M., Ibrahim, L., Casanova, J. L., Puel, A., & Bouaziz, J. D. (2015). Posaconazole treatment of extensive skin and nail dermatophytosis due to autosomal recessive deficiency of CARD9. JAMA dermatology, 151(2), 192–194. https://doi.org/10.1001/jamadermatol.2014.2154
- Tirado-Sánchez A, Ponce RM, Bonifaz A. Majocchi granuloma (dermatophytic granuloma): updated therapeuticoptions. Curr Fungal Infect Rep. 2015;9(4):204–12.
